Para los menos atentos los colores de los LEDs se obtienen de la misma manera que en las lámparas comunes: la luz es blanca y simplemente se pone un plástico del color deseado para tener luz roja, verde, amarilla o cualquier otra. De hecho, el LED no es una lámpara incandescente, pero si un semiconductor y el color de su luz está determinado por un proceso mucho más complejo que explicamos en este artículo. Entender cómo la producción de luz se produce en un simple LED puede ser muy importante para que los lectores entiendan más sobre la física de los semiconductores y que rige el funcionamiento de un gran número de dispositivos que van desde los simples diodos hasta los láseres.
La luz nada más es de lo que radiación electromagnética, es decidir, está formada por ondas cuyas frecuencias difieren de las señales comunes de radio, TV, radar y otros que estamos acostumbrados a utilizar en electrónica, sólo por su frecuencia. En la figura 1 tenemos la localización de la gama visible, o sea, de las frecuencias que nuestros ojos pueden ver, en el espectro electromagnético.
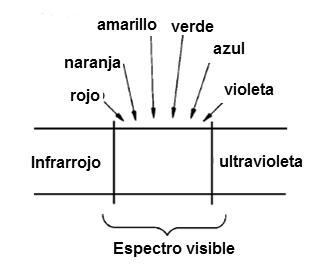
Como el lector puede percibir, en esta gama, las diferentes longitudes de onda o frecuencias determinan también el tipo de sensación que nuestro ojo va a tener en relación el color de la luz.
Así, las frecuencias más bajas y por lo tanto las longitudes de onda mayores corresponden a la luz roja y naranja, mientras que las longitudes de onda menores y frecuencias más altas corresponden a la radiación azul y violeta.
La manera más simple para conseguir la luz y por lo tanto la emisión de la radiación electromagnética y por el calentamiento. Calentando un cuerpo, sus átomos vibran en todos los frecuencias posibles que emite la luz de todos los colores que se mezclan. El sol opera de esta forma y una lámpara común de filamento también.
En el sol la alta temperatura agita los átomos de las sustancias que lo forman de tal manera que ellos pasan a emitir radiación lo mismo ocurriendo con el filamento de una lámpara incandescente cuando es recorrido por una corriente eléctrica, como se muestra en la figura 2.
La emisión de la radiación de estos cuerpos es hecha desproporcionalmente. Esto significa que cada átomo al ser revuelto emite una pequeña porción de radiación en una longitud de onda o frecuencia diferente.
Es interesante notar que la energía emitida en estas condiciones también tiene una cuantidad mínima, como el átomo que es la porción mínima de la materia. Eso significa que los átomos excitados siempre emiten esas porciones mínimas, que son denominadas "Quantum" de energía. El plural de "Quantum", que es una palabra latina, es "Quanta" y la teoría que explica cómo ellas se comportan es la teoría cuántica.
Así que cuando los átomos son revueltos por el calor, cada uno emite una frecuencia diferente de energía "quantum". El resultado de esto es que en el solo tenemos un tipo de radiación, pero más bien una mezcla que cubre todo el espectro visible y mismo parte de lo que no podemos ver como de las radiaciones infrarroja y ultravioleta, como se muestra en la figura 3.
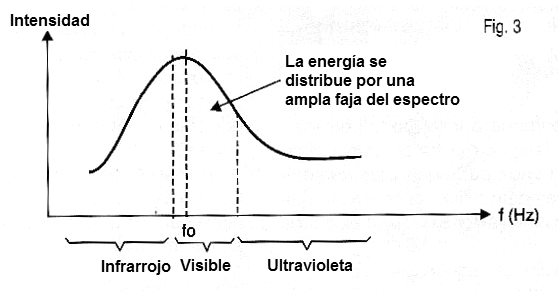
Si la distribución de energía emitida o sea, la cantidad de quanta es el más o menos uniforme en el sector del espectro que podemos ver, la mezcla nos dará la sensación de una luz blanca.
Sin embargo, la distribución de esta energía emitida varía dependiendo de la temperatura del cuerpo. Un cuerpo más caliente tiende a emitir más partículas de frecuencias más altas. Por esta razón, un cuerpo muy caliente brilla con luz azulada. Un cuerpo más frio, por ejemplo, una plancha caliente, brilla con luz rojiza, como se muestra en la figura 4.
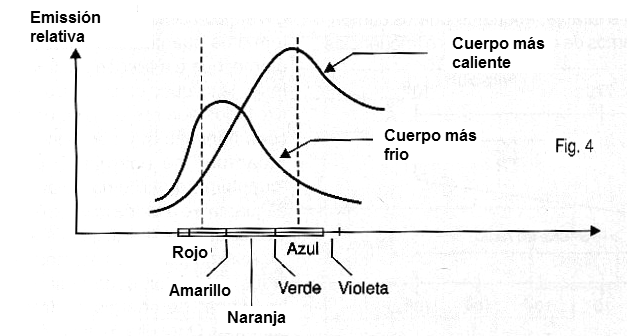
Un físico llamado Boltzman estableció en una formula la distribución de la emisión de esta radiación en función de la temperatura para un cuerpo negro.
Es interesante de una emisión de luz blanca, que configura todas las longitudes de onda como la del sol es que nos permite ver los colores de la naturaleza.
Así lo que pasa es que si iluminamos un objeto y el refleja apenas la luz azul, absorbiendo las demás, él nos aparecerá azul a nosotros, como se muestra en la figura 5.
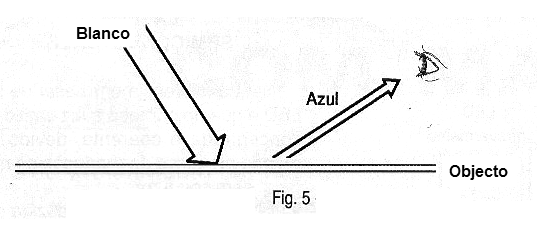
Los objetos que vemos en la naturaleza cuando son iluminados por la luz del sol o una lámpara común aparecen en los colores que tiene porque reflejan las frecuencias que determinan estos colores.
Si encendemos un objeto verde con una fuente de luz que emite radiación correspondiente a la luz roja, el objeto se verá completamente negro.
Vea entonces que podemos hablar de los tipos de emisiones de luz:
El de las fuentes como el sol y una lámpara común que en realidad tienen todos ellos frecuencias posibles y que por lo tanto cubren una gama larga del espectro y fuentes que pueden emitir luz desde una sola frecuencia.
En la electrónica podemos asociar estas fuentes de una sola frecuencia a un transmisor bien sintonizado, mientras que la luz que cubre todo el espectro sería un emisor de ruido.
Decimos que las fuentes de luz que emiten radiación de una sola frecuencia o color son Monocromáticas. Los LEDs son fuentes monocromáticas porque producen una luz por un proceso diferente al que vimos para el sol y para una lámpara común. Considere cómo funcionan los LEDs:
NIVELES DE ENERGÍA Y LUZ MONOCROMÁTICA
Cualquier material, incluyendo los semiconductores, cuando se calienta emite luz por la agitación de sus átomos.
Sin embargo, los materiales ciertos pueden emitir sin luz se ralentizan, esta es, pueden emitir luz aunque sea fría, por un proceso llamad luminiscencia.
La luminiscencia de ciertos materiales ha sido conoce desde 1889, pero sólo si se ha utilizado Más en la electrónica en la creación de varios dispositivos.
Un tipo de luminiscencia es la que ocurre cuando un rayo de electrones golpea una cubierta de fósforo en la pantalla de un televisor. La luminiscencia es explicada cómo sigue:
Los electrones que rotan alrededor de un átomo o hacen en órbitas bien establecidas que fijan niveles de energía, como se muestra en la figura 6.
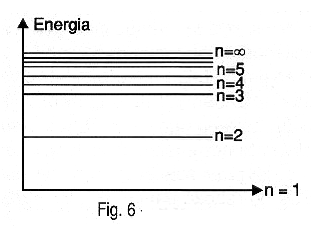
Un átomo no puede absorber para una breve energía instantánea y cuando algo un electrón "salta" de su órbita que mueve a otro alto nivel de energía. En otras palabras, la Energy es almacena potencialmente en la position del electrón en su órbita.
Cuando el electrón, una fracción de segundo después de absorber la energía, vuelve para su órbita normal, la energía absorbida y devuelta, como se muestra en la figura 7.
La energía devuelta es un quantum de radiación electromagnética cuya frecuencia dependerá del "salto" del electrón, o sea , de la energía que tiene para devolver.
Los niveles de energía que un electrón puede tomar en un átomo depende de la naturaleza de este átomo, o sea, del material que representa. Así que para cada tipo de átomo los electrones pueden dar saltos definidos, lo que significa que solo ellos pueden devolver la energía bajo la forma de radiación electromagnética de frecuencia muy bien definida.
Si la gama de energía que el electrón devuelve es entre 3800 y 7500 Angstroms, la energía se manifiesta en forma de luz visible y el material en el que esto ocurre pasa a emitir luz.
Existen diversas maneras de excitar un material para que el absorba y luego emita la energía en forma de radiación electromagnética.
El movimiento de una corriente en una dirección directa de una junción semiconductora, por ejemplo, un diodo común, como se muestra en la figura 8, es una de ellas.
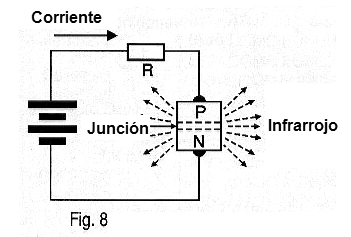
Sin embargo, en un diodo común, la energía emitida concentrados en la gama infrarroja (que no podemos ver) y su intensidad es demasiado pequeña.
Esta radiación tiene su frecuencia determinada precisamente por la naturaleza del semiconductor material utilizado en diodos que es silicio.
Para obtener la radiación a frecuencias más altas que la del infrarrojo se puede usar otros materiales semiconductores que tienen diferentes niveles de energía e incluidos para cambiar los niveles por la adición de impurezas.
Así, como el Arseneto de Galio (GaAs) nos las arreglamos para conseguir un desempeño mayor en el proceso, pero todavía en la gama infrarroja.
Añadiendo fosforo o indio al arseniuro de galio podemos obtener frecuencias mayores y el semiconductor ya emite luz en el gama de rojo, amarillo, naranja, verde, azul y llegar hasta el violeta y ultravioleta, como se muestra en la tabla de la figura 9.
Vea por este gráfico que las curvas emisión de los dispositivos obtenidos de esta manera que son los LEDs (Light-Emitting Diodes o Diodos Emisores de Luz ) son bastante estrechas, lo que significa que son fuentes de luz monocromáticas.
Para obtener frecuencias altas que es de la luz verde, se ha utilizado una nueva sustancia. Es el Carboneto de Silicio (SIC) que tiene propiedades luminiscentes conocidas desde los comienzos de siglo.(En la época en que el artículo fue escrito.)
Sin embargo, la obtención de cristal semiconductores puro de esta sustancia fue un difícil superar hace poco tiempo.
El Carboneto del Silicio bajo la forma de semiconductor puede, al ser despertado eléctricamente, emite la luz no solo en la gama de frecuencias que corresponde al azul cómo llegar hasta mismo al violeta.
De esta manera, con esta nueva sustancia, se pueden fabricar LEDs azules y violetas que ya están en el mercado. La sustancia que es el emisión de luz en la gama de violeta es el Nitrato de Silicio (SiN) que ya se utiliza en la fabricación de LEDs.
En la figura 10 tenemos la estructura de un LED de este tipo, en el cual se observa la existencia de tres tipos de materiales.
Junto con la juntura pn epitaxial tenemos un substrato de SIC que excita en la conducción y que causa la emisión de luz.
En la figura 11 tenemos la emisión curva de un LED azul observando que es mucho más ancha que la de los LEDs comunes de Arseneto de Galio, dadas las características del material semiconductor.
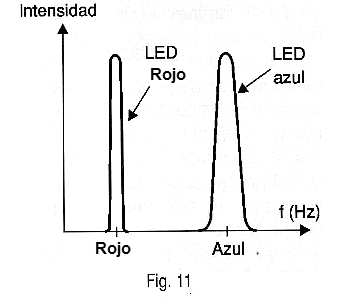
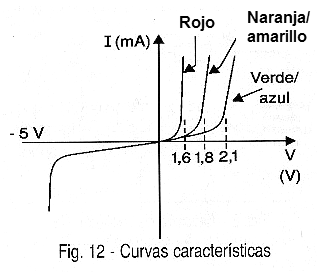
Los LEDs azules y violetas tienen una curva característica similar a la de cualquier diodo y LED común, apenas con la "rodilla", o sea, el punto del inicio de la conducción a una tensión ligeramente superior: 2,5 V.
Esta curva característica se muestra en la figura 12, y ella nos muestra que el uso de un LED de este tipo en nada difiere de dos LEDs comunes, requiriendo la colocación de una resistor de limitación de corriente en serie.
LASERS SEMICONDUCTORES
Lo que diferencia un láser de un LED es que en el láser la luz emitida es concentrada y coherente, debido al proceso de producción en el material semiconductor.
En un LED la luz es producida por una excitación incontrolada de los átomos que, al recibir y devolver la energía emite luz en cualquier momento y en cualquier dirección.
En un láser los átomos reciben la excitación de tal modo que hay un fenómeno llamado "inversión de populación", o sea, que en un instante dado tengamos más átomos excitados que sin excitación.
Así, cuando un átomo devuelve su energía forma una cantidad de luz, este Quanta sirve para excitar otros átomos energizados, lo que les obliga para retornar su energía en una especie de reacción en cadena, que se muestra en la figura 13.
El resultado es que la devolución de la energía absorbida se hace de un excitado y coordenada, que resulta en la emisión de luz concentrada y coherente.
Un semiconductor en el material desempaquetado permite el retorno sea más controlada y la emisión se produce en una sola dirección.
Pero de la misma manera que en los LEDs la frecuencia y por lo tanto el color de la luz emitida depende de la naturaleza del material y hoy en día ya son disponibles los LASERs semiconductores de diferentes longitudes de onda.









