Sin pilas o baterías la mayoría de los aparatos electrónicos portátiles no podrían funcionar. Saber como funcionan, los tipos disponibles en el mercado, y algunos cuidados relativos a su uso, es tan importante como conocer el propio equipa que alimentan.
Este artículo es de 1989. Las tecnologías actuales no son abordadas.
Convertir la energía liberada en una reacción química en energía eléctrica: ésta es la función de una pila.
Esta energía disponible puede entonces utilizarse para poner en funcionamiento los más diversos aparatos que van desde linternas, radios portátiles, hasta sistemas de señalización y transmisores en satélites artificiales.
El tipo de pila que siempre tomamos como base para explicar su principio de funcionamiento se llama "Pila de Volta", nombre en homenaje de su inventor, Alejandro Volta.
La misma consistía simplemente en una estructura como la que aparece en la figura 1, en que discos de cobre y zinc se alternaban, teniendo entre ellos discos de tejido embebido en una solución de ácido sulfúrico en agua.
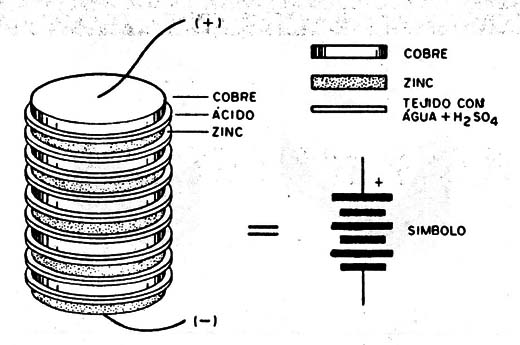
Cada par de discos puede proporcionar una tensión en abierto del orden de 1,2 a 1,6V siendo el polo positivo el disco de cobre y el polo negativo el disco de zinc. La tensión disponible, naturalmente, seria dada por la cantidad de pares de discos montados en la estructura.
A partir de este primer tipo; de pila, cuyo desempeño y durabilidad dejan mucho que desear, se produjo una larga evolución. De este modo, lo que tenemos actualmente son pilas y batería bien distintas, tanto en la forma como en el desempeño, pero que en cuanto al principio de funcionamiento no se apartan mucho del tipo básico.
Antes de analizar todos los tipos de pilas comunes con que podemos contar en estos momentos y sus principales características, tenemos que hacer inicialmente algunas consideraciones sobre los términos usados en este articulo.
Comencemos por dejar bien claro que existe una diferencia entre lo que llamamos pila y lo que llamamos batería.
La pila o célula es la unidad de provisión de energía, o sea, el conjunto básico de elementos que permite obtener energía a partir de reacciones químicas.
La batería consiste en una asociación de células o pilas, con el fin de obtener una cantidad de energía mayor, que una pila o célula única no conseguiria (figura 2).
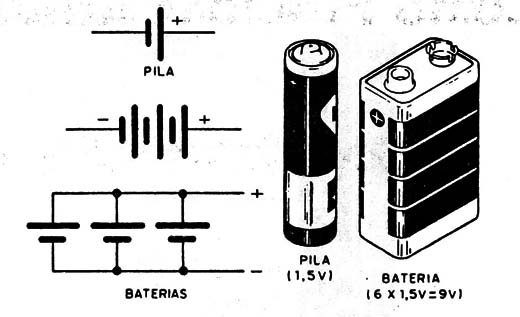
Como ejemplo, podemos decir que una pila de linterna es realmente una pila porque consiste en una unidad de provisión de energía con un electrodo positivo, uno negativo y una solución activa.
La batería de un automóvil está formada por una cierta cantidad de células que son asociadas de modo de obtener una tensión mayor.
A continuación debemos aclarar la diferencia entre lo que llamamos células primarias y células secundarias.
Las pilas de linterna comunes son células primarias, pues al ser fabricadas ya poseen energía, pero sólo por una vez, o sea, después de descargadas no pueden recibir más una nueva carga.
Las células secundarias, al ser fabricadas, no pueden proveer inmediatamente energía, y precisan antes de pasar por un proceso de carga. Y después que se descargan, pueden ser recargadas un cierto número de veces antes de terminar su vida útil.
En la figura 3 mostramos los ciclos de vida de estas pilas o células.
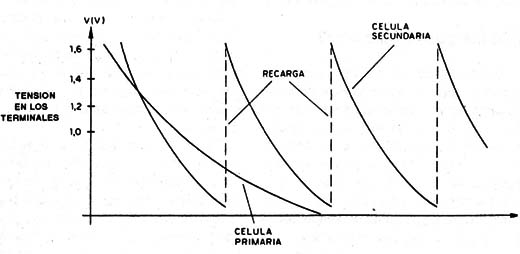
La célula primaria tiene apenas un ciclo de operación en su vida útil, mientras que la secundaria tiene varios.
En la misma figura mostramos los tipos de células más comunes de los dos grupos. Cambiando ahora de tema:
¿si existen varios tipos de, pilas y baterías, cómo saber cuál debe usarse en cada aplicación? Esto es lo que intentaremos responder de ahora en adelante, analizando el funcionamiento y las características de las principales pilas disponibles en nuestro mercado.
Pila seca, Ieclanché o zinc-carbono
Sin duda esta es la pila más común de todas. Es Ia pila seca, o pila de radio, que encontramos en venta en las principales tiendas, supermercados, quioscos y demás locales.
Se fabrican en tres tamaños básicos, AA, D y C, según el uso, conocidos también como "pequeñas", "medianas“ y “grandes", aunque hay tamaños menos comunes. En la figura 4 tenemos la estructura interna de una pila de este tipo, a partir de la cual analizaremos su funcionamiento.
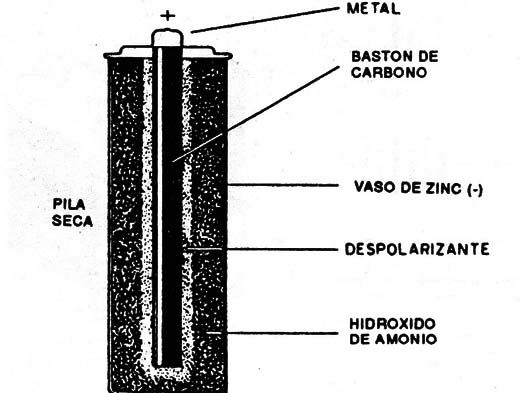
La cubierta externa de la pila es un vasito de zinc que también sirve como electrodo negativo. Un bastón de carbono, que tiene en la parte superior un casquito de metal, forma el electrodo positivo, en la parte central.
Alrededor del electrodo central, que es el bastón, existe una mezcla de carbono en polvo y dióxido de manganeso que se denomina despolarizante. La finalidad de esta sustancia es absorber las burbujas de hidrógeno que se pueden formar durante el funcionamiento de la pila y que, con su presión, podrían hacerla explotar, eso sin hablar del aumento de la resistencia interna
EI restante espacio interno del vasito se llena con una pasta de cloruro de amonio, que es el electrolito, o sea, la sustancia activa de la pila.
La tensión encontrada en los terminales de esta pila, sin carga, es del orden de 1,5 a 1,6V. La corriente máxima depende de su tamaño; pilas mayores pueden proporcionar más corriente.
Cuando están en uso, las pilas de este tipo presentan una curva característica del tipo que muestra la figura 5.

A cada ciclo de uso, la tensión cae gradualmente, hasta el momento en que es desconectada. Cuando esto ocurre, la tensión sube, pero no vuelve al valor inicial. Con el tiempo, la pila cada vez más pasa a proveer tensiones menores a la carga hasta el punto en que no se la puede usar más.
Para una pila común, se puede obtener un buen número de ciclos de funcionamiento si la corriente exigida por la carga no es elevada. Es el tipo de funcionamiento que se nota en radios portátiles y otros aparatos de bajo consumo. Si las corrientes exigidas fueran elevadas, se debe usar el tipo "Heavy Duty" (Servicio Pesado), proyectada para proporcionar muchos ciclos de alto consumo, sin problemas. Es lo que ocurre en la alimentación de grabadores pequeños, linternas y juguetes donde el consumo es mayor.
La resistencia interna, al aumentar, hace que la capacidad de una pila para producir corriente se vea reducida.
Las pilas secas, como de otros tipos, también sienten los efectos de la temperatura. La temperatura ideal de funcionamiento es la situada entre 20 y 27ºC.
Por debajo y encima ocurren diversos tipos de problemas. Por debajo de 15ºC, por ejemplo, tanto la tensión como la capacidad de corriente caen acentuadamente, y por debajo de 5º C su uso se vuelve prácticamente imposible.
Otro tipo de problema que ocurre con este tipo de pila es el "vaciamiento". De hecho, el vaso externo, que es el electrodo negativo, puede ser consumido totalmente en las condiciones en que se exigen grandes corrientes, lo que ocurre principalmente en las linternas, y esto permite que el electrolito, bastante corrosivo, se salga.
EI resultado no necesita explicarse para los que ya han visto una linterna o una radio "comidas" por una pila en estas condiciones.
En las aplicaciones en que se exigen tensiones mayores con corrientes todavía no muy altas, se pueden montar las pilas secas en cubiertas únicas formando baterías.
En la figura 6 mostramos dos tipos de los más comunes.
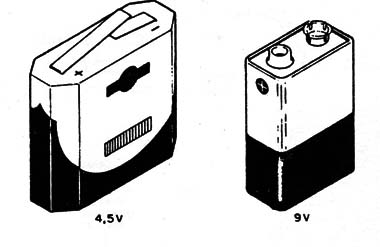
La primera es la batería de 4,5V formada por 3 pilas de 1,5V conectadas en serie. Estas son cilíndricas, como las pilas comunes que se venden por separado. En las baterías de 9V tenemos un montaje diferente. Son células planas, apiladas de modo que forman en serie un conjunto que resulte en la tensión deseada.
Recordamos que las baterías de de este tipo son dispositivos de baja corriente, y por lo tanto se gastan enseguida si se las usa inadecuadamente.
¿Se las puede reactivar?
Muchos lectores deben conocer la creencia popular según la cual colocando en la heladera o en agua caliente una pila de este tipo, la misma "se carga", pudiendo usársela todavía por más tiempo.
En verdad, lo que ocurre en este caso no es realmente una recarga, sino una reactivación. En el caso de la heladera, influye mucho más el tiempo que la pila queda en reposo, permitiendo así que el despolarizante entre en acción eliminando los gases formados, que la temperatura propiamente dicha; en cuanto al caso del agua caliente, realmente se puede con ella reactivar lo que resta de la solución, permitiendo así el funcionamiento de la misma por algún tiempo más.
Pilas alcalinas
Es un tipo de célula que puede proveer mucha más energía, en comparación con las pilas secas, y se las recomienda para los casos en que se exige mayor corriente, y mayor autonomía, todo en un volumen menor.
En la figura 7 tenemos un gráfico en que se compara el desempeño de este tipo de pila con una pila seca común.
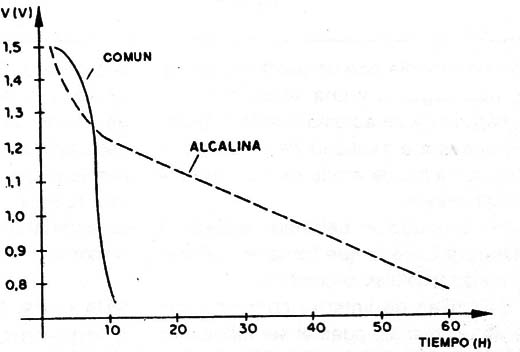
Como podemos ver por el gráfico, la durabilidad de una pila alcalina, en las mismas condiciones de funcionamiento que una pila seca común, es muy superior. Su costo más alto puede perfectamente ser compensado por la mayor durabilidad;
Es importante resaltar que el factor tiempo por factor capacidad de corriente no corresponde de una forma lineal.
Esto quiere decir que si una pila puede funcionar durante una hora proporcionando corriente de 100 mA, la misma no funcionará 10 horas si la corriente fuera de 10 mA. Para una corriente menor durante mayor tiempo, la durabilidad puede ser extendida. Este factor es muy importante en la elección de una pila para una aplicación.
En estas pilas la cubierta externa es de acero, consistiendo también en el polo negativo, mientras que el electrodo positivo consiste en bolitas de zinc. El electrolito es hidróxido de potasio, una sustancia alcalina, de ahí el nombre de la pila. Recordamos que este tipo de pila es una célula primaria, y por lo tanto no permite la recarga.
Batería plomo-ácido
Pasamos ahora a una fuente de energía secundaria, ya que este tipo de batería puede ser recargada.
En la figura 8 tenemos su estructura simplificada, donde mostramos sólo una célula. Se sumergen dos placas de plomo en una solución de ácido sulfúrico, que es el electrolito.
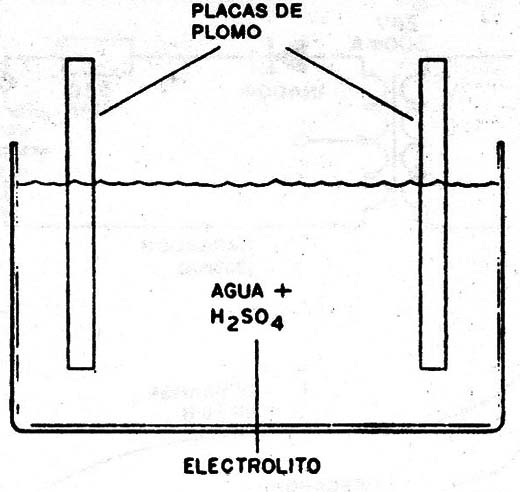
Cuando se carga la batería, una de las placas permanece como plomo, mientras que la otra se modifica químicamente.
Cada célula de este tipo manifiesta una tensión sin carga entre sus terminales entre 2,3 a 2,4V cuando está plenamente cargada. Con carga, esta tensión cae a valores entre 2 y 2,2V.
Asociando entonces 6 de estas células tenemos la conocida batería de 12V usada en los autos (figura 9).
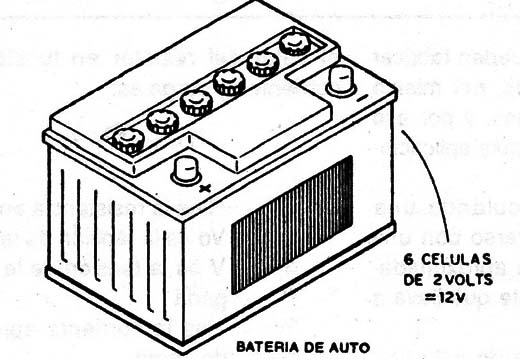
La capacidad de una batería de este tipo es normalmente especificada en amperes-hora (Ah) para una descarga de 10 horas.
Una batería de auto de 40 Ah, por ejemplo, puede proveer una corriente de 4A durante 10 horas. Mientras tanto, en este caso, la relación entre el factor tiempo por el factor corriente no es lineal.
En una descarga rápida, con corriente de 1%, por ejemplo, la durabilidad de la batería ya no será de 4 horas, sino menor, mientras que, con una descarga bajo menor corriente, el tiempo podrá ser mayor del calculado.
En condiciones de operación en cortos intervalos de tiempo, como en el caso del arranque de un auto, estas baterías pueden proporcionar corrientes muy elevadas, del orden de hasta centenares de amperes.
EI estado de carga o descarga de una batería de este tipo as dado. por la densidad del electrolito, la cual puede ser medida por un aparato denominado densímetro, que aparece en la figura 10.
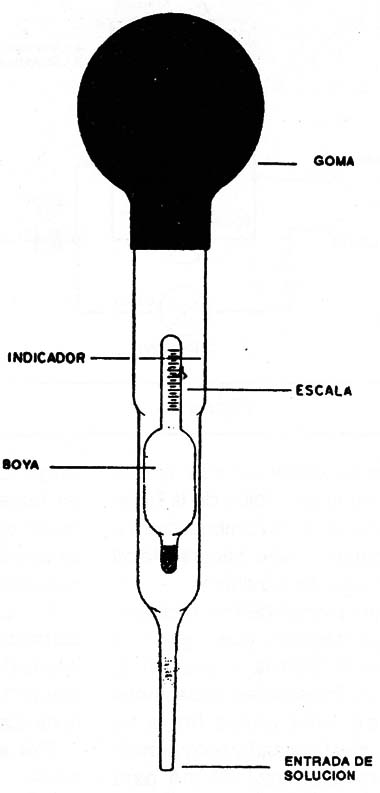
En las condiciones de plena carga, el densímetro acusará valores entre 1,21 y 1,27 para el electrolito, dependiendo del tipo de batería (típicamente 1,26 para autos). La carga de una batería debe hacerse con cuidado.
Carga de baterías plomo-ácido
Para una batería inicialmente descargada, se recomienda que la corriente de carga sea de 1A para 5Ah de capacidad, lo que nos lleva a una corriente de 5A para una batería de auto común de 40 Ah.
Esta carga debe durar hasta que el electrolito comience a burbujear y la tensión entre los terminales llegue a 2,3V para cada elemento. Cuando esto ocurre, la corriente debe ser reducida a 1A para cada. 25Ah de capacidad, lo que lleva a aproximadamente 2A para una batería común de carro, hasta el fin.
Esta es la llamada carga rápida, que puede hacerse con el circuito de la figura 11, bastante económico, donde el diodo para la red de 220V debe tener una tensión inversa de pico de 400V y una corriente de 10 A.
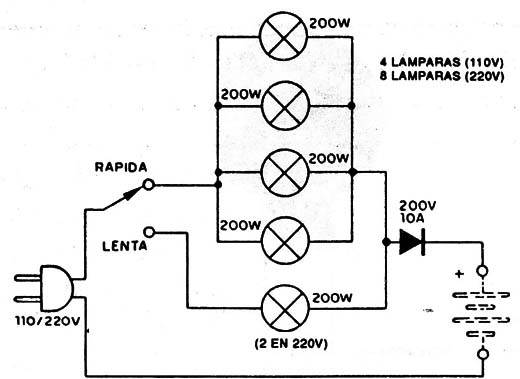
Las lámparas incandescentes están siendo descontinuadas no se fabricando más.
Es importante observar que el gas que burbujea en el electrolito de la batería es hidrógeno, que es combustible. La carga de la batería debe hacerse lejos del fuego y en lugares ventilados.
La carga que mencionamos más arriba es la carga “rápida", que reduce la durabilidad de la batería y que por lo tanto sólo debe hacerse en situaciones excepcionales. Una carga lenta es mucho mejor, siendo usada normalmente una corriente de hasta 30 mA para cada 100 Ah. Una batería de auto en carga lenta se podría hacer con 120 mA de corriente, a largo plazo.
Pilas y baterías de níquel-cadmio
Este es un tipo muy importante de célula secundaria que puede por lo tanto ser cargada, y que comienza a difundir- se bastante en las aplicaciones electrónicas. Lo que ocurre es que el electrolito liquido y la necesidad de ventilación permanente (a causa del hidrógeno) impiden que las baterías de plomo-ácido se usen en otra posición que no sea la vertical, lo que no ocurre con las de nicádmio (níquel-cadmio).
Estas pilas poseen como electrolito una solución de hidróxido de potasio, mientras que los electrodos son formados por acero perforado. En el electrodo positivo tenemos, para llenarlo, polvo de cadmio finamente dividido, mezclado con un poco de hierro para evitar Ia pérdida de la porosidad.
En la figura 12 mostramos Ia curva de descarga típica de una batería de este tipo.
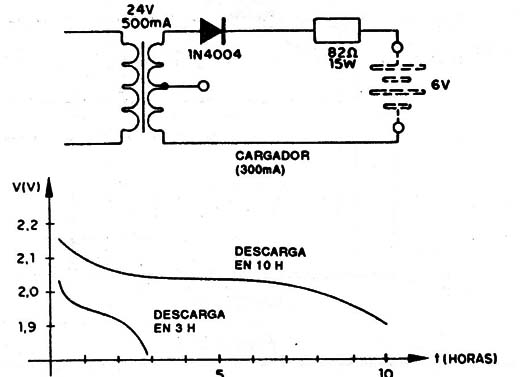
En las condiciones de circuito abierto (sin carga) la tensión de una célula de nicádmio es de 1,3 a 1,4V, pero esta tensión cae a 1,2V con una carga. Estas baterías se pueden fabricar en tamaños muy pequeños, del mismo modo que las pilas comunes, y por eso se pueden usar en las mismas aplicaciones, con ventaja.
La carga se hace circulando una corriente en el sentido inverso con una intensidad que equivale a aproximadamente 1,5 veces la corriente que lleva a la descarga en 10 horas.
Por ejemplo, si una pila de este tipo, se descarga en 10 horas cuando solicitamos una corriente de 100 mA (1 Ah de capacidad), entonces su carga ideal se hace con una corriente de 1,5 x 100 mA 150 mA.
Para cargar este tipo de pila se pueden usar fuentes reguladas (fuentes de corriente constante), siendo algunas bastante sofisticadas, pero de un modo simple se puede obtener dentro de buenos limites una corriente constante para la carga de una batería de nicádmio.
Este método aparece en la figura 13 y consiste en la utilización de una fuente con una tensión mucho mayor que la de la pila o batería a ser cargada, teniendo en serie un resistor que reduzca la corriente al valor deseado.
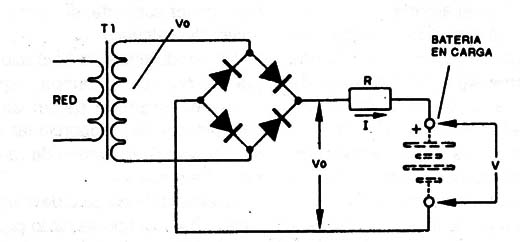
Una fórmula simple para determinar el valor del resistor en función de la corriente de carga es:
R = (Vo – V ) / I
R es la resistencia en Ω
Vo es la tensión de la fuente
V es la tensión de la pila cargada
l es la corriente aproximada de carga
La disipación del resistor es dada por:
P = R x l2
P es la potencia en watts que se debe disipar
R es la resistencia en Ω
l es la corriente en amperes
En la práctica, el resistor debe tener una capacidad de disipación por lo menos dos veces mayor.
Para los lectores interesadas en más detalles sobre un montaje con este fin, les recomendamos leer diversos proyectos de cargadores que se encuentran en este sitio.
Atención: Al usar baterías de nicádmio, tenga cuidado de no poner en corto sus terminales, pues las mismas pueden explotar.




